
近日,研究组在催化机制与酶工程领域取得重要突破,研究成果以“Mechanistic insights into the substrate promiscuity of α-ketoacid decarboxylases for enhanced higher-alcohol biosynthesis”为题,正式发表于国际期刊 ACS Sustainable Chemistry & Engineering。该研究系统揭示了一类重要工业酶——α-酮酸脱羧酶(α-KDC)识别底物并表现出底物广谱性的结构基础,并成功实现其底物选择性的定向调控,显著提升了2-苯乙醇(2-PE)的微生物合成效率。
高级醇是一类具有高能量密度和低水溶性的化合物,广泛用于燃料、化工和香精香料等领域。在微生物合成高级醇的途径中,α-酮酸脱羧酶催化不可逆的脱羧反应,是整个通路的“限速引擎”。然而,这类酶天然具有底物广谱性——既是优势,使其能够催化多种底物,也是挑战,容易导致代谢分流和产物选择性下降。如何在保留催化效率的同时提升底物选择性,是该领域的核心科学问题。
本研究以来源于Enterobacter的KDC4427酶为研究对象,成功解析了KDC4427及其与天然底物苯丙酮酸(PPA)和吲哚丙酮酸(IPA)的复合物结构,首次揭示了该酶中由保守 HH-motif与ThDP辅因子4′-氨基共同构成的“氧阴离子孔”,精确识别底物的 α-酮酸极性头部;同时发现一个宽敞、疏水的底物结合口袋,能够灵活容纳不同结构的疏水尾部,揭示了底物广谱性的结构基础。理论计算进一步表明,IPA与 PPA在结合亲和力和催化能垒上存在显著差异,其中脱羧步骤(TS4)为整个反应的主要限速步,解释了二者在不同催化速率上的差异。基于结构信息,团队对底物结合口袋中的关键残基(如Q383、V467、I471、I542)进行了饱和突变,筛选出一系列选择性显著改变的突变体。其中,Q383E 突变体 对 PPA 的选择性提高 2倍。将Q383E 突变体引入大肠杆菌的2-PE 合成途径后,摇瓶产量提升约16%(达242.4 mg/L)。在5 L发酵罐中采用原位萃取工艺,该工程菌在24小时内实现了27.9 g/L的 2-PE 产量,转化效率达80.7%,为目前已知的E. coli中2-PE最高产量之一。
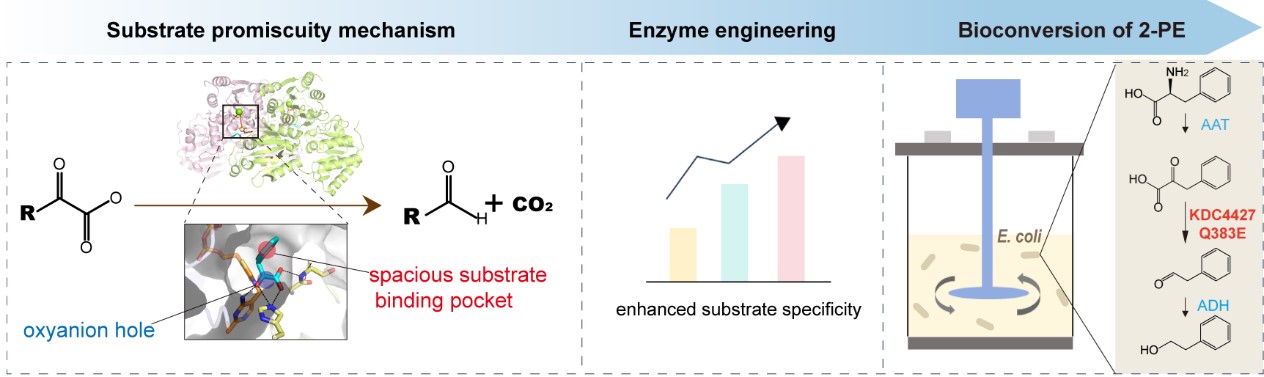
本研究从原子水平解答了“KDC 如何识别并催化多种底物”这一关键科学问题,提出了“极性头部精确锚定 + 疏水尾部宽松匹配”的双重识别模型。该机制不仅为理解酶的底物广谱性提供了新范式,也为高级醇合成途径关键酶的理性设计提供了系统性框架。未来,研究组将进一步探索该酶在非天然高级醇、药物中间体等绿色合成中的应用潜力,并持续推进微生物细胞工厂的整体优化。
本文通讯作者为中国科学院青岛生物能源与过程研究所张海波研究员,上述工作得到国家重点研发计划、国家自然科学基金、山东省自然基金、山东省泰山学者、青岛新能源山东省实验室开放课题等项目资助。
原文链接:https://pubs.acs.org/doi/10.1021/acssuschemeng.5c13943
